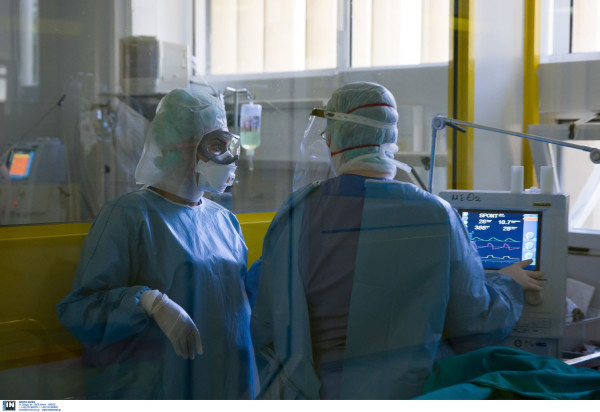
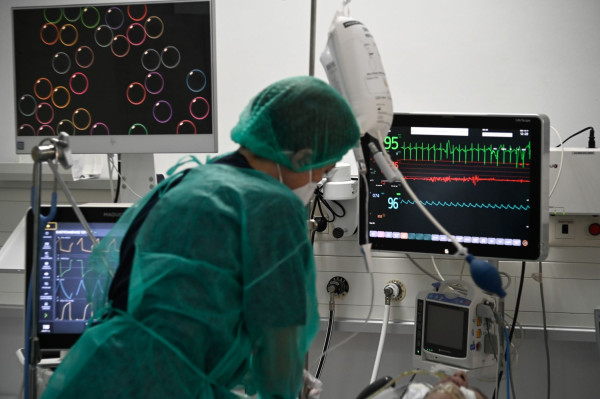
Στο επίκεντρο συζητήσεων έχει βρεθεί το τελευταίο διάστημα ένα από τα βασικά φάρμακα που χρησιμοποιούν νοσοκομειακοί γιατροί στη θεραπευτική τους φαρέτρα κατά της COVID-19. Η δεξαμεθαζόνη και η ρεμδεσιβίρη (remdesivir) αποτελούν τα δύο βασικά «πυρομαχικά» που έχουν στη διάθεση τους οι γιατροί και στη χώρα μας για να αντιμετωπίσουν την επέλαση του ιού στον οργανισμό του κάθε ασθενούς.
Με την κούρσα για την ανάπτυξη εμβολίου να βρίσκεται σε πλήρη εξέλιξη και παρότι τα πρώτα εμβόλια αναμένεται να είναι διαθέσιμα τέλη 2020 – αρχές 2021, εκτιμάται ότι θα χρειαστούν μήνες, αν όχι χρόνος για να αρχίσουν να καταγράφονται σημαντικά ποσοστά ανοσίας στον πληθυσμό από τον εμβολιασμό. Έτσι, τα φάρμακα, σε συνδυασμό με τα περιοριστικά μέτρα και τις πρακτικές ατομικής προστασίας, αναδεικνύονται στη βασική άμυνα των γιατρών κατά της COVID-19 και του συστήματος υγείας για τη διασφάλιση των αντοχών του. Για αυτό άλλωστε, παράλληλα με την ανάπτυξη των εμβολίων, η επιστημονική κοινότητα και η φαρμακοβιομηχανία αναζητούν περισσότερες θεραπευτικές επιλογές κατά της νόσου.
«Το lockdown μάς δίνει μια δυνατότητα να κερδίσουμε χρόνο, έτσι ώστε να βρούμε καινούργιες θεραπείες και να έχουμε και το χρόνο να εμβολιαστούμε. Σήμερα έχουμε καλύτερα θεραπευτικά πρωτόκολλα από ότι είχαμε τον Απρίλιο. Ξέρουμε ότι τόσο η ρεμδεσιβίρη όσο και η δεξαμεθαζόνη, πραγματικά βοηθούν τους ασθενείς μας», ανέφερε στο πλαίσιο της τακτικής ενημέρωσης για την πορεία της πανδημίας η Καθηγήτρια Βάνα Παπαευαγγέλου, στις 13 Νοεμβρίου.
Παρά την ευρεία χρήση τους, όμως, δύο φορείς έθεσαν ερωτηματικά γύρω από το κατά πόσο η ρεμδεσιβίρη βελτιώνει σημαντικά την υγεία των ασθενών με COVID-19.
Αρχικά, ενστάσεις εξέφρασε η Ευρωπαϊκή Ένωση Εντατικής Φροντίδας. Με δηλώσεις του στο Reuters o πρόεδρος της Jozef Kesecio η ρεμδεσιβίρη δεν θα πρέπει να χρησιμοποιείτε τακτικά σε ασθενείς με COVID-19, λαμβάνοντας υπόψη τα νέα προσωρινά δεδομένα από τη δοκιμή SOLIDARITY του ΠΟΥ.

Ο Παγκόσμιος Οργανισμός Υγείας (ΠΟΥ) ακολούθησε μερικές ημέρες μετά, αναφέροντας πως το αντιιικό φάρμακο ρεμδεσιβίρη δεν συστήνεται σε ασθενείς που εισάγονται στο νοσοκομείο με κορονοϊό. Η επιτροπή εμπειρογνωμόνων κατέληξε στο συμπέρασμα ότι δεν υπάρχουν στοιχεία βάσει των διαθέσιμων δεδομένων που βελτιώνουν σημαντικά αποτελέσματα των ασθενών. Άρα, το remdesivir δεν έχει ουσιαστική επίδραση στη θνησιμότητα ή σε άλλα σημαντικά αποτελέσματα για τους ασθενείς, όπως η ανάγκη για μηχανική υποστήριξη ή χρόνο για κλινική βελτίωση.
Σε ό,τι αφορά τη θέση του ΠΟΥ θα πρέπει να τονίσουμε άλλα δύο σημεία. Ο ίδιος ο Οργανισμός αναγνώρισε ότι, η βεβαιότητα των αποδεικτικών στοιχείων είναι χαμηλή και ότι όπως δεν αποδείχθηκε η σημαντική βελτίωση έτσι δεν αποδείχθηκε ότι η ρεμδεσιβίρη δεν έχει κανένα όφελος. Αλλά δεδομένης της υπολειπόμενης πιθανότητας σημαντικής βλάβης, καθώς και του σχετικά υψηλού κόστους και των επιπτώσεων στους πόρους η σύσταση χρήση της δεν είναι κατάλληλη.
Τα κλινικά οφέλη
Ωστόσο, στην αντίπερα όχθη από τον ΠΟΥ φαίνεται να στέκονται FDA και EMA, ο Αμερικανικός και Ευρωπαϊκός Οργανισμός Φαρμάκων, αντίστοιχα. Οι δύο κορυφαίοι φορείς, που είναι και υπεύθυνοι για την έγκριση των φαρμάκων που χορηγούνται στους πολίτες των ΗΠΑ και της Ε.Ε. πήραν σαφής αποστάσεις από την τοποθέτηση του Παγκόσμιου Οργανισμού Υγείας.
Είναι ενδεικτικό ότι o FDA ενέκρινε στις 25 Νοεμβρίου τη χρήση του remdesivir στη θεραπεία της COVID-19 αναφέροντας μεταξύ άλλων ότι τα αποτελέσματα της μελέτης SOLIDARITY του ΠΟΥ δεν αντικρούουν τα ευρήματα των κλινικών μελετών που στοιχειοθέτησαν την απόφαση πλήρους έγκρισης της ρεμδεσιβίρης. Η μελέτη έδειξε ότι μειώνει το χρόνο της ανάρρωσης και τη βελτίωση της πιθανότητας κλινικής βελτίωσης των ασθενών.
Αντίστοιχα, ο EMA χορήγησε την υπό όρους άδεια κυκλοφορίας στο remdesivir στις 3 Ιουλίου 2020, βάσει των δεδομένων από τη μελέτη που απέδειξε την κλινική αποτελεσματικότητα και ασφάλεια του remdesivir για τη θεραπεία ασθενών με COVID-19 πνευμονία, οι οποίοι χρειάζονται συμπληρωματικό οξυγόνο.
Τον Οκτώβριο ακολούθησε η υπογραφή «συμφωνίας κοινής προμήθειας» μεταξύ της Gilead Sciences, που παράγει το φάρμακο και της Ευρωπαϊκής Επιτροπής, ώστε να επιτραπεί η ταχεία και ισότιμη πρόσβαση στο φάρμακο. Μια ημέρα μετά η εταιρεία υπέγραψε συμφωνία με το ΙΦΕΤ, που εξασφάλισε την ευρεία πρόσβαση στο remdesivir σε κατάλληλους ασθενείς με COVID-19 στη χώρα μας. Θυμίζουμε, βέβαια, ασθενείς στην Ελλάδα είχαν πρόσβαση στο φάρμακο νωρίτερα, στο πλαίσιο συμμετοχής τους στην κλινική μελέτη.
Αντίστοιχα, τη χορήγηση της ρεμδεσιβίρης έχουν συστήσει και το Εθνικό Ινστιτούτο Υγείας (NIH), η Επιστημονική Εταιρεία Λοιμώξεων (IDSA) στις ΗΠΑ και φορείς σε Βρετανία, Γερμανία και Ιαπωνία.
Σχολιάζοντας, πάντως, τη σύσταση του Παγκόσμιου Οργανισμού Υγείας, ο Ευρωπαϊκός Οργανισμός Φαρμάκων ανέφερε πως θα τη θέσει σε αξιολόγηση, προσθέτοντας όμως πως «σύμφωνα με τον ΠΟΥ, η βεβαιότητα των αποτελεσμάτων της μετα-ανάλυσης είναι χαμηλή και τα στοιχεία δεν αποδεικνύουν ότι η ρεμδεσιβίρη δεν έχει όφελος». Σε ό,τι αφορά μάλιστα την ασφάλεια του remdesivir, το φάρμακο είναι «καλώς αποδεκτό με ανάλογα ποσοστά παρενεργειών τόσο για τη ρεμδεσιβίρη όσο και για το placebo».