Το φάρμακο της Regeneron, REGN-COV2, ένας συνδυασμός των μονοκλωνικών αντισωμάτων casirivimab και imdevimab, το οποίο έχει λάβει άδεια έκτακτης χρήσης απο τον αμερικανικό Οργανισμό Τροφίμων και Φαρμάκων (FDA), θα είναι η πρώτη θεραπεία της κατηγορίας που θα χορηγήθει σε ασθενείς στην Ελλάδα.
Όπως ανέφερε μιλώντας στο ραδιόφωνο του ΣΚΑΙ o πρόεδρος του ΕΟΦ, το φάρμακο αυτό θα χορηγηθεί σε ασθενείς με συγκεκριμένα χαρακτηριστικά που θα συμμετέχουν σε σχετική κλινική μελέτη για τη χορήγηση του. Ειδικότερα, το κοκτέιλ αντισωμάτων αφορά ασθενείς με ήπια έως μέτρια μορφή της νόσου COVID-19, άνω των 12 ετών, που κρίνονται υψηλού κινδύνου για επιδείνωση ή/και νοσηλεία.
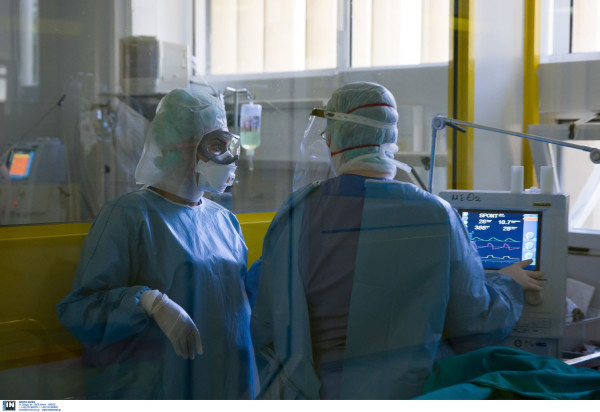
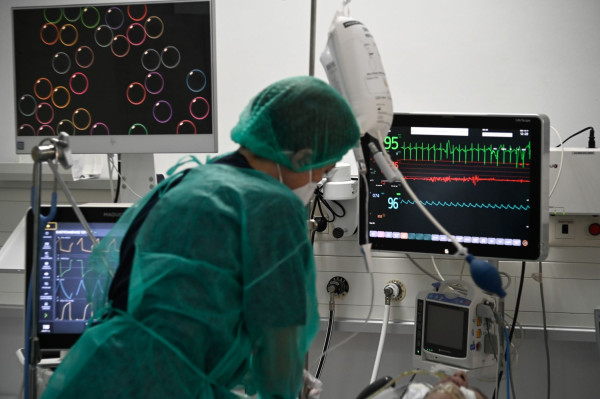
Πρέπει να διευκρινίσουμε ότι πρόκειται για φάρμακο νοσοκομειακής χρήσης. Κατ'επέκταση αν και αφορά ασθενείς των οποίων η νόσος COVID-19 δεν έχει εξελιχθεί στη σοβαρή της μορφή, είτε νοσηλεύονται είτε παρακολουθούνται κατ'οίκον, η χορήγηση του φαρμάκου σε κάθε περίπτωση θα πρέπει γίνεται σε νοσοκομειακό περιβάλλον.
Οι ασθενείς υψηλού κινδύνου είναι όσοι είναι παχύσαρκοι, με δείκτη μάζα σώματος άνω των 35, άτομα άνω των 65 ετών ή με συνοδά νοσήματα όπως η χρόνια νεφρική νόσος, διαβήτης, καρδιαγγειακή νόσος ή αναπνευστικά προβλήματα. Δεδομένα από την κλινική μελέτη φάσης 1/ 2 με τη συμμετοχή 799 ασθενών έδειξε ότι το κοκτέιλ της Regeneron μπορεί να μειώσει το ιικό φορτίο σε σημαντικό βαθμό, σε σχέση με το placebo.
Κυρίως, όμως, ήταν μικρότερα τα ποσοστά επισκέψεων σε νοσοκομείων στους ασθενείς που έλαβαν το συνδυασμό REGN-COV2, μέσα σε 28 ημέρες. Μάλιστα, «το όφελος ήταν μεγαλύτερο σε ασθενείς υψηλού ρίσκο, λόγω υψηλού ιικού φορτίου, αναποτελεσματική ανοσολογική απόκριση ή προϋπάρχοντες παράγοντες κινδύνου», όπως ανέφερε ο Γιώργος Γιανκόπουλος, Επιστημονικός Διευθυντής της Regeneron.
Εκατοντάδες χιλιάδες δόσεις θεραπείας του κορονοϊού ετοιμάζονται για το Γενάρη του 2021
Η παραγωγή των αντισωμάτων είναι ιδιαίτερως δύσκολη διαδικασία και προκειμένου να ανταπεξέλθει στη ζήτηση η Regeneron συνεργάζεται με τη Roche. Ειδικότερα, η Regeneron θα χειριστεί τις πωλήσεις των ΗΠΑ, ενώ την ευθύνη για την αγορά εκτός ΗΠΑ έχει αναλάβει η Roche. Συνιδρυτής, πρόεδρος και επικεφαλής επιστήμονας της Regeneron είναι ο ελληνοαμερικανός Τζορτζ Γιανκόπουλος.
Στάση αναμονής για άλλες δύο θεραπείες κατά του COVID-19
Την ίδια στιγμή φαίνεται να έχουν παγώσει οι προσπάθειες χορήγησης σε ασθενείς στην Ελλάδα άλλων δύο θεραπειών κατά της COVID-19, που έχει αναπτύξει η Eli-Lilly και έχουν λάβει άδεια έκτακτης χρήσης από τον FDA.
Η μια εξ αυτών είναι το bamlanivimab, που μπορεί να χορηγηθεί σε άτομα που έχουν διαγνωστεί με ήπια έως μέτρια νόσο COVID-19, αλλά και για άτομα που ανήκουν σε ευπαθή ομάδα και βρίσκονται θετικοί στον κορονοϊό SARS-COV-2, πριν την εμφάνιση των συμπτώματων και έως και 10 ημέρες αφού παρουσιαστεί και σαφώς πριν κριθεί απαραίτητη η νοσηλεία τους και η υποστήριξη της αναπνοής τους.
Η δεύτερη θεραπεία είναι το baricitinib, του οποίου μάλιστα η χορήγηση μπορεί να γίνει και ταχύτερα, καθώς το εν λόγω φάρμακο έχει αρχική ένδειξη και στη χώρα μας για τη χρήση σε ασθενείς με Ρευματοειδή Αρθρίτιδα. Μάλιστα, το baricitinib έχει πάρει τιμή, έχει περάσει από τις διαδικασίες αξιολόγησης και διαπραγμάτευσης και αναμένεται άμεσα να ενταχθεί στη Θετική Λίστα, τον κατάλογο με τα φάρμακα που αποζημιώνονται από την κοινωνική ασφάλιση.
Σύμφωνα, όμως, με πληροφορίες, ο μόνος τρόπος χορήγησης ενός φαρμάκου που έχει λάβει άδεια έκτακτης χρήσης από τον FDA είναι μέσω της ένταξης του σε πρωτόκολλο κλινικής μελέτης, καθώς αυτή η άδεια δεν συνιστά τυπικά οριστική και πλήρη έγκριση ενός φαρμάκου. Η φαρμακευτική εταιρεία που έχει αναπτύξει αυτές τις δύο θεραπείες δεν έχει αυτή τη στη στιγμή ανοικτό πρωτόκολλο κλινικής μελέτης.
Για να μπορέσει ένα φάρμακο να χορηγηθεί μέσω προγράμματος είτε πρώιμης πρόσβασης είτε παρηγορητικής χρήσης θα πρέπει να έχει εγκριθεί από τον ΕΜΑ ή έστω τον FDA, μια εκ των ρυθμιστικών αρχών, δηλαδη.
Μάλιστα, παρότι φέρεται να υπάρχει διάταξη που προβλέπει την έκτακτη εισαγωγή κατ'εξαίρεση θεραπειών, που δεν κυκλοφορούν αλλά κρίνονται απαραίτητες για τη μείωση της διασποράς μολυσματικών παραγόντων, η νομική υπηρεσία του ΕΟΦ φέρεται να ξεκαθαρίζει πως δεν μπορεί να δώσει το πράσινο φως για τη χορήγηση των δύο αυτών φαρμάκων, εφόσον δεν διαθέτουν πλήρη άδεια.