Η εταιρεία είχε τέσσερις διαφορετικούς υποψηφίους εμβολίων. Αφού εξέτασαν προκλινικά και κλινικά δεδομένα από τις κλινικές δοκιμές της Φάσης Ι / ΙΙ και συζητήθηκαν με την Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) και τους ρυθμιστές άλλων χωρών, επέλεξαν το BNT162b2 για να συμμετάσχουν σε μεγαλύτερες μελέτες.
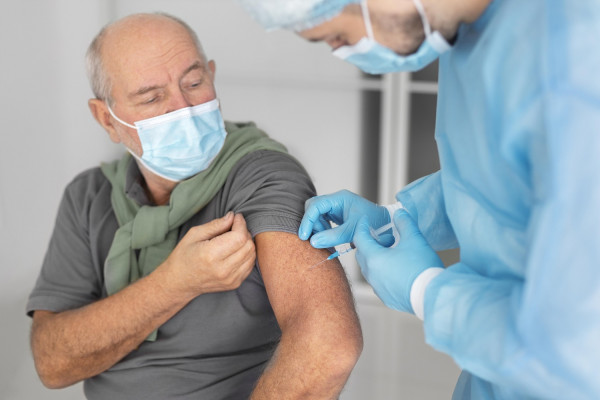
Το εμβόλιο θα χορηγηθεί σε 30 μικρογραμμάρια με ένα σχήμα δύο δόσεων. Το εμβόλιο είναι ένα προϊόν mRNA, με το mRNA να κωδικοποιεί την πρωτεϊνη ακίδα που χρησιμοποιει ο SARS-CoV-2 για να συνδεθεί με τα ανθρώπινα κύτταρα.
«Η έναρξη της δοκιμής Φάσης II / III είναι ένα σημαντικό βήμα προόδου στην πορεία μας προς την παροχή ενός πιθανού εμβολίου για την καταπολέμηση της συνεχιζόμενης πανδημίας COVID-19 και ανυπομονούμε να δημιουργήσουμε επιπλέον δεδομένα καθώς προχωρά το πρόγραμμα» δήλωσε ο Kathrin U. Jansen, ανώτερος αντιπρόεδρος και επικεφαλής της Έρευνας & Ανάπτυξης Εμβολίων για την Pfizer
Τα τέσσερα εμβόλια των εταιρειών περιορίστηκαν στους δύο καλύτερους υποψήφιους, BNT162b1 και BNT162b2 με βάση την ασφάλεια και την ανοσοαπόκριση. Μετά από διεξοδική ανάλυση των δεδομένων, το BNT162b2 επιλέχθηκε ως ο καλύτερος υποψήφιος για να προχωρήσει. Εκτός από τα υψηλά επίπεδα εξουδετερωτικών αντισωμάτων σε πολλά διαφορετικά ζωικά μοντέλα, οι υποψήφιοι προκάλεσαν ευνοϊκές αντιδράσεις CD4 + και CD8 + Τ-κυττάρων για ιό, καθώς και έδειξαν προστατευτικά αποτελέσματα σε ένα μοντέλο πρόκλησης πρωτεύοντος SARS-CoV-2, δηλαδή , έδωσαν τα εμβόλια σε πρωτεύοντα, στη συνέχεια τους ένεσαν με τον ιό και φάνηκε να αποτρέπει τη μόλυνση.
Η δοκιμή Φάσης II / III θα διεξαχθεί σε 120 κλινικές περιοχές σε όλο τον κόσμο, εκτός από την Κίνα, αλλά θα περιλαμβάνει 39 πολιτείες στις ΗΠΑ. Αργεντινή, Βραζιλία και Γερμανία θα συμπεριληφθούν στη δοκιμή.
Ο Philip Dormitzer, αντιπρόεδρος της Pfizer και επικεφαλής των εμβολίων, δήλωσε στη STAT ότι επειδή το υποψήφιο εμβόλιο περιλαμβάνει περισσότερη από τις πρωτεΐνες αξίδες, φαίνεται να δημιουργεί μια ισχυρότερη ανοσοαπόκριση, η οποία θα πρέπει να σημαίνει λιγότερη μεταβλητότητα στην ανταπόκριση των ασθενών. Φαίνεται επίσης ότι προκαλεί λιγότερες παρενέργειες. «Φαινόταν λίγο πιο ήπια», είπε. «Υπήρχαν λιγότερες αντιδράσεις στην ανοσοποίηση, και αυτό ήταν ένα σημαντικό σημάδι υπέρ της».
Ξεκίνησαν οι δοκιμές
Η κλινική δοκιμή ξεκίνησε χθες και θα επιστρατεύσει περίπου 30.000 υγιείς εθελοντές ηλικίας μεταξύ 18 και 85 ετών. Θα τυχαιοποιηθούν 1: 1 για να λάβουν το εμβόλιο ή ένα εικονικό φάρμακο. Τα κύρια τελικά σημεία της δοκιμής θα είναι η πρόληψη του COVID-19 σε εκείνους που δεν έχουν μολυνθεί από το SARS-CoV-2 πριν από την ανοσοποίηση και θα αποτρέψουν το COVID-19 ανεξάρτητα από το εάν οι συμμετέχοντες είχαν προηγουμένως μολυνθεί από τον ιό. Τα δευτερεύοντα τελικά σημεία περιλαμβάνουν την πρόληψη της σοβαρής COVID-19. Θα αξιολογήσει επίσης την πρόληψη της μόλυνσης από τον ιό.
«Σήμερα, ξεκινάμε την παγκόσμια μελέτη μας που θα περιλαμβάνει έως και 30.000 συμμετέχοντες», δήλωσε ο Ugur Sahin, διευθύνων σύμβουλος και συνιδρυτής της BioNTech. «Επιλέξαμε το BNT172b2 ως τον κύριο υποψήφιο για αυτήν τη δοκιμή Φάσης II / III μετά από επιμελή αξιολόγηση του συνόλου των δεδομένων που έχουν παραχθεί μέχρι στιγμής. Αυτή η απόφαση αντικατοπτρίζει τον πρωταρχικό μας στόχο να διαθέσουμε ένα καλά ανεκτό, πολύ αποτελεσματικό εμβόλιο στην αγορά το συντομότερο δυνατό, ενώ θα συνεχίσουμε να αξιολογούμε τους άλλους υποψήφιους εμβολίων ως μέρος ενός διαφοροποιημένου χαρτοφυλακίου εμβολίων COVID-19. Έχουν γίνει πολλά βήματα προς αυτό το σημαντικό ορόσημο και θα θέλαμε να ευχαριστήσουμε όλους όσοι συμμετείχαν για την εξαιρετική τους αφοσίωση».
ΠΗΓΗ: biospace